Перевод А. Белоусов, sarcoidosis@yandex.ru
Глава 19
Клиническая полноценность ядерных методов визуализации при саркоидозе
J. Mana, M. van Kroonenburgh
Dept of Internal Medicine, Bellvitge Institute of Medical Research, Bellvitge Hospital, University of Barcelona, Barcelona, Spain, and Dept of Nuclear Medicine/Sarcoidosis Management Centre, University Hospital Maastricht, Maastricht, The Netherlands.
Correspondence: J. Mana, Servicio de Medicina Interna, Hospital Universitario de Bellvitge, Feixa Llarga s/n, L'Hospitalet de Llobregat, 08907 Barcelona, Spain. Fax: 34 932607967; E-mail: jmana@csub.scs.es
Ядерные методы визуализации играют важную роль в оценке и лечении пациентов с саркоидозом. Для этих целей, начиная с конца 1970-х, использовались разнообразные радиофармпрепараты. Настоящая глава сосредоточена на использовании этих радиофармпрепаратов, методах визуализации, их роли и клинической ценности при саркоидозе. Обсуждается корреляция с другими методами визуализации, биохимическими параметрами и исследованиями функции легких. Интеграция доступных в настоящее время данных и собственного опыта, позволила разработать алгоритм, на основании которого авторы предлагают руководящие принципы, сосредоточенные на оптимальном использовании ядерных методов визуализации при начальном исследовании пациентов с саркоидозом.
Сцинтиграфия с галлием-67
Радиоизотоп галлий-67 накапливается в злокачественных опухолях, включая лимфомы, а также при воспалительных процессах [1]. Наиболее вероятно, в гранулематозной ткани 67Ga поглощается активизированными макрофагами. Хотя поглощение 67Ga обычно подавляется кортикостероидами, сообщалось о персистировании поглощения у пациентов с активным саркоидозом, у которых проводилось лечение [2].
Чувствительность сцинтиграфии с 67Ga при обнаружении легочного саркоидоза располагается в диапазоне 60-90 %. Однако, специфичность этого метода относительно мала, потому что большинство интерстициальных болезней легкого демонстрируют положительные результаты при сцинтиграфии с 67Ga [1]. Наиболее обычно, поглощение 67Ga при саркоидозе является внутригрудным и обычно показывает двустороннюю внутригрудную и паратрахеальную лимфаденопатию и/или поглощение в легочной паренхиме. Сцинтиграфия всего тела с 67Ga полезна для изучения степени и распределения болезни, позволяет обнаружить присутствие воспалительной активности при клинически незаметном поражении органов и позволяет идентифицировать внелегочные участки для проведения биопсии [3, 4]. О внелегочном накоплении 67Ga сообщалось для многих органов (рис. 1), что подтверждает системный характер саркоидоза [1, 4-6].

Рис. 1. Сцинтиграфия с 67Ga демонстрирует множественные очаги поглощения в черепе, нижней челюсти, обеих околоушных железах, цервикальных и надключичных лимфатическиих узлах у пациента с положительными результатами биопсии цервикальных лимфатических узлов: a) фронтальный вид, b) латеральный вид. Изображения воспроизведены из [5] с разрешения авторов.
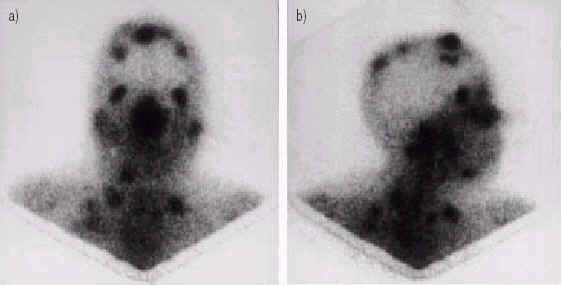
Sulavik с колл. [7] сообщили о некоторых комбинациях различных паттернов поглощения 67Ga, как о характеристиках саркоидоза. Изображение, произведенное поглощением 67Ga в паратрахеальных и грудных лимфатических узлах, походящее на греческую букву лямбда, было названо лямбда-паттерном. Изображение, произведенное поглощением 67Ga в слезных и околоушных железах, походящее на морду медведя панда, было названо панда-паттерном. Лямбда-паттерн был замечен у 72 % пациентов с саркоидозом, панда-паттерн у 79 % и оба паттерна одновременно у 62 %. Однако, панда-паттерн не является специфическим для саркоидоза, так как он также наблюдается у ВИЧ-положительных пациентов, пациентов с синдромом Сьёгрена, после облучения головы или шеи при лечении лимфомы, при реакции ''трансплантант против хозяина'', ревматоидном артрите и системной красной волчанке [7, 8]. Israel с колл. [3] обнаружили более низкую чувствительность лямбда-паттерна (29 %) и панда-паттерна (13 %) у пациентов с саркоидозом. Рис. 2 показывет лямбда- и панда-паттерн у пациента с синдромом Лёфгрена [9].
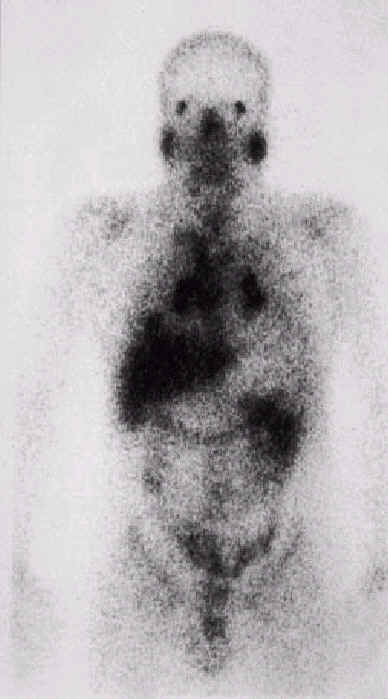
Рис. 2. Сцинтиграфия с 67Ga показывет лямбда- и панда-паттерн у пациента с синдромом Лёфгрена. Изображение воспроизведенно из [9] с разрешения авторов.
Несколько исследований сосредоточились на роли сцинтиграфии с 67Ga в прогнозе саркоидоза. Niden с колл. [10] сообщили, что меньшая степень легочного поглощения 67Ga указывет на лучший прогноз. Аналогично, восстановление и сохранение нормальных результатов сцинтиграфии с 67Ga в течение терапии были хорошим прогностическим признаком, так как такие пациенты не имели ухудшения легочной функции. Baughman с колл. [11] сообщили, что 68 % пациентов с положительными результатами сцинтиграфии легких с 67Ga, имели ухудшение болезни через 2 года, принимая во внимание, что отрицательные результаты указывали на малую вероятность активности болезни через 2 года.
Другие исследования не смогли подтвердить эти результаты [12, 13]. В мультицентровом Европейском исследовании 632 пациентов [14], не наблюдалось строгой корреляции между накопленим 67Ga и присутствим ненормальностей на рентгенограмме легких (Таблица 1). Согласно этим результатам, сцинтиграфия с 67Ga была более точна при обнаружении присутствия внутригрудной болезни в существенном числе случаев с нормальной рентгенограммой. Однако, 23 % случаев с признаками внутригрудной болезни на рентгенограмме, не имели накопления 67Ga. Кроме того, сцинтиграфия с 67Ga была более чувствительной, чем рентгенограмма для обнаружения ухудшения и предсказания рецидивов при наблюдении пациентов без лечения.
Таблица 1. Поглощение 67Ga у нелеченных пациентов в различных рентгенографических стадиях саркоидоза
| Стадия | Пациенты, n | Увеличенное поглощение 67Ga, (%) | Отсутствие увеличенного поглощения 67Ga, (%) | |
| Медиастинальное и/или легочное | Легочное | |||
| I | 82 | 36 (43.9) | 10 (12.2) | 46 (56.1) |
| II | 190 | 164 (86.3) | 40 (21.1) | 26 (13.7) |
| II | 248 | 213 (85.9) | 160 (64.5) | 35 (14.1) |
| IV | 112 | 71 (63.4) | 65 (58.0) | 41 (36.6) |
| Всего | 632 | 484 (76.6) | 265 (41.9)# | 148 (23.4) |
# число пациентов с увеличенным легочным поглощением 67Ga выражено как процент от числа пациентов с увеличенным медиастинальным и/или легочным поглощением 67Ga - 54.8 %. Воспроизведено из [14] с разрешения авторов.
Некоторые исследования сравнили компьютерную томографию с высоким разрешением (КТВР) с сцинтиграфией легких с 67Ga и обнаружили слабую корреляцию между этими двумя методами. Lynch с колл. [15] обнаружил, что пять пациентов с положительными результатом сцинтиграфии с 67Ga имели некоторую степень легочного поражения на КТВР, но два из пяти пациентов с нормальными результатами сцинтиграфии с 67Ga, имели паренхиматозную болезнь легкого на КТВР.
Кроме того, узловые повреждения на КТВР не коррелировали с результатами сцинтиграфии с 67Ga. Bergin с колл. [16] сообщили о слабой корреляции между двумя методами, хотя участки паренхиматозного поражения на КТ соответствовали местоположению фокальных областей накопления 67Ga. Однако, Leung с колл. [17] сообщил о хорошей корреляции между результатами КТВР и сцинтиграфии с 67Ga у 29 пациентов с легочным саркоидозом. Современные исследования показали, что КТВР имеет больше возможностей для оценки патологических изменений и функционального ухудшения, связанных с воспалительной активностью саркоидоза [18-20]. Drent с колл. [21] сообщили о хорошей корреляции между легочными ненормальностями на КТВР, но не на рентгенограмме, с ухудшением функции легкого и, особенно, с нарушениями газообмена. Поэтому, считается, что для оценки воспалительной активности и серьезности внутригрудного поражения при саркоидозе, КТВР более полезна, чем сцинтиграфия с 67Ga.
В вышеупомянутом Европейском исследовании [14], серологический уровень ангиотензинпревращающего фермента (АПФ) был увеличен у 29 % пациентов с отрицательными результатами сцинтиграфии; это измерение было более чувствительным чем сцинтиграфия легкого с 67Ga только у 7 % из всех нелеченных пациентов. Напротив, результаты сцинтиграфии с 67Ga были положительны у 58 % пациентов с нормальным уровнем АПФ и были более чувствительны чем уровень АПФ у 30 % нелеченных пациентов. Следовательно, сцинтиграфия с 67Ga была более чувствительным измерением, чем уровень АПФ при обнаружении активного саркоидоза, хотя уровень АПФ в небольшом числе случаев имел преимущество. Другие авторы также подтвердили более высокую чувствительность сцинтиграфии с 67Ga по сравнению с уровнем АПФ, как индикатора активности болезни [2, 22-24], хотя некоторые считают, что уровень АПФ - более специфический маркер [23]. Напротив, другие исследования обнаружили сильную корреляцию между обоими методами [25, 26]. Эти различия можно было бы объяснить фактом, что эти два метода могут характеризовать различные аспекты формирования гранулемы и обнаружение ингибиторов АПФ в сыворотке 30 % пациентов с саркоидозом, могли бы объяснить нормальный уровень АПФ в некоторых случаях активного саркоидоза [26].
В Европейском исследовании [14], уровень АПФ и накопление 67Ga в течение кортикостероидной терапии активного легочного саркоидоза были увеличены у 17 и 38 % пациентов, соответственно. Через один месяц после прекращения терапии, эти проценты увеличились до 70 и 59 %, что говорит, что уровень АПФ позволяет обнаружить рецидивы лучше, чем сцинтиграфия с 67Ga. Другое исследование обнаружило, что сцинтиграфия с 67Ga была более чувствительной чем бронхоальвеолярный лаваж (БАЛ) при обнаружении изменений в течение кортикостероидной терапии [27]. Была описана хорошая корреляция между степенью накопления 67Ga и увеличением жизненной емкости легких после лечения [28].
Однако, накопление 67Ga не было ценным при предсказании ответа на лечение [12]. Turner-Warwick с колл. [29] сообщили, что сцинтиграфия с 67Ga, индекс лимфоцитов в БАЛ и измерение уровня АПФ были не более чувствительны, чем рентгенограмма и исследование функции легких при контроле пациентов в течение терапии. Патология сцинтиграфии с 67Ga сама по себе не является показанием для терапии. Аналогично, присутствие новых очагов накопления 67Ga в течение или после прекращения кортикостероидной терапии может быть полезным при подтверждении рецидива в сомнительных случаях, но не является показанием для повторного лечения кортикостероидами. Однако, Nosal с колл. [22] сообщили, что комбинация уровня АПФ и сцинтиграфии с 67Ga имеет специфичность 99 % и считают, что если результаты обеих экспертиз отрицательны, диагноз саркоидоз является в высокой степени маловероятным.
Некоторые авторы сообщили о сильной корреляции между паренхиматозным накоплением 67Ga и интенсивностью альвеолита, определяемого числом T-лимфоцитов в ЖБАЛ [30-32], хотя другие исследования не обнаружили подобной корреляции [2]. Одна из возможных причин отсутствия корреляции - то, что ЖБАЛ отражает интенсивность лимфоцитарного альвеолита, который может преобладать в ранних стадиях болезни, принимая во внимание, что результаты сцинтиграфии с 67Ga отражают присутствие активизированных макрофагов и гранулем, которые обычно преобладают в более поздних стадиях.
При легочном саркоидозе, результаты исследования функции легких в присутствии альвеолита могут быть нормальными. Line с колл. [31] обнаружили слабую корреляцию между степенью альвеолита, результатами сцинтиграфии с 67Ga и степенью ухудшения функции легкого. Напротив, некоторые исследования обнаружили, что даже небольшое накопление 67Ga в легочной паренхиме было связано с некоторой степенью ухудшения функции легкого, принимая во внимание, что другие показали хорошую корреляцию между степенью накопления 67Ga и увеличением жизненной емкости после кортикостероидной терапии [28].
Вследствие малой чувствительности и специфичности, сцинтиграфия с 67Ga имеет ограниченную ценность при оценке активности, постановке диагноза и лечении саркоидоза. Поэтому, в настоящее время сцинтиграфия с 67Ga не рекомендуется при начальной оценке саркоидоза. Сцинтиграфия с 67Ga при саркоидозе может быть полезной при постановке диагноза, определении степени и локализации болезни в диагностически трудных случаях. Пациенты с нормальной рентгенограммой и клинической картиной, суггестивной для изолированного внелегочного саркоидоза, например увеита, болезни центральной нервной системы или моновисцерального гранулематоза неизвестного происхождения, особенно гранулематозов печени и лимфатических узлов, могут иметь пользу при сцинтиграфии с 67Ga. Обнаружение типичного лямбда- и/или панда-паттерна поддерживает диагноз и указывает на необходимость гистологического подтверждения [8]. Сцинтиграфия всего тела также может обнаружить другие очаги клинически незаметного внелегочного накопления 67Ga, указывая на участки для проведения биопсии [3, 4].
Аналогично, в случаях синдрома Лёфгрена и бессимптомной стадии I с вызывающей сомнение внутригрудной лимфаденопатией на рентгенограмме не подтвержденной гистологически, обнаружение лямбда-паттерна при сцинтиграфии с 67Ga может вносить вклад в подтверждение диагноза [33]. Однако, нормальные результаты сцинтиграфии с 67Ga не устраняют возможности присутствия гранулем в любом органе. Сцинтиграфия с 67Ga не была полезной при предсказании прогноза и не должна использоваться как индикатор для начала терапии [12, 13]. Однако, она может быть полезной при дифференцировании фиброзной болезни легкого от активной, помогать при принятии решения о прекращении или продолжении кортикостероидной терапии, подтверждать развитие рецидива после прекращения терапии в сомнительных случаях и помогать при оценке активности болезни перед трансплантацией легкого [1].
Сцинтиграфия с таллием-201
Радиоизотопный таллий-201 накапливается в нормальных миокардиальных клетках. Сцинтиграфия с 201Tl позволяет производить атравматичную оценку распределения миокардиальной перфузии. При кардиосаркоидозе, сцинтиграфия с 201Tl , выполненная в состоянии покоя обычно показывает сегментальные области уменьшенной перфузии в миокарде, которые соответствуют областям фиброгранулематозных изменений [34, 35]. В отсутствии болезни коронарных артерий, эти дефекты при саркоидозе предполагают поражение сердца, особенно, если дефекты исчезают или уменьшаются в размере при стрессовой сцинтиграфии с 201Tl (при нагрузке или после внутривенного введения дипиридамола) [34, 36-38]. Это явление, называемое обратным распределением (reverse distribution), предполагает присутствие гранулем в пределах миокарда и полезно при дифференцировании кардиосаркоидоза от миокардиальной ишемии [35, 36]. Однако, этот эффект наблюдается не всегда и не специфичен для кардиосаркоидоза, так как также может происходить при других кардиомиопатиях [35]. Tellier с колл. [39] сообщили, что дефекты перфузии были частично или полностью обратимы после внутривенного введения дипиридамола, мощного сосудорасширяющего средства, улучшающего коронарную микроциркуляцию, и считают, что механизмом нарушения перфузии может быть присутствие обратимых нарушений на капиллярном уровне, скорее чем миокардиальные гранулемы или фиброз. Однако, из-за возможности присутствия небольших фокальных повреждений, нормальные результаты сцинтиграфии с 201Tl не исключают возможности присутствия кардиосаркоидоза [34].
Kinney с колл. [40] отметили присутствие ненормальностей при сцинтиграфии с 201Tl у более 30 % пациентов с саркоидозом без клинически подозреваемого поражения сердца. Sharma с колл. [35] обнаружил патологию результатов сцинтиграфии с 201Tl у 34 % пациентов с системным саркоидозом и наблюдал, что все дефекты левого желудочка уменьшились при стрессовой сцинтиграфии. Haywood с колл. [36] обнаружили дефекты левого или правого желудочка у 37 % пациентов, у которых эхокардиография не смогла показать ненормальности сокращения желудочков. В исследовании 41 пациента с саркоидозом, была выполнена миокардиальная эмиссионная компьютерная томография одиночных фотонов (SPECT). Патологические результаты были обнаружены у 26 пациентов [38].
Комбинация сцинтиграфии с 201Tl и 67Ga и особенно SPECT, может улучшить диагностирование кардиосаркоидоза [41, 42]. Однако, Okayama с колл. [43] сообщили, что когда сцинтиграфия с 201Tl показывала миокардиальные дефекты, сцинтиграфии с 67Ga не добавляла диагностической информации; однако, этот метод позволяет прогнозировать эффективность лечения кортикостероидами. Однако, Kinney и Caldwell [44] считают, что результаты сцинтиграфии с 201Tl не имеют прогностической ценности, хотя периодическая оценка дефектов перфузии была полезна при контроле прогресса миокардиального саркоидоза и его ответа на терапию [36, 37].
Сцинтиграфия с 201Tl не должна использоваться для поиска присутствия поражения сердца у пациентов с саркоидозом без миокардиальных симптомов [1, 9]. Кроме кардиосаркоидоза, существенное накопление 201Tl при саркоидозе наблюдается в костных повреждениях [45]. Другие методы оценки перфузии включают сцинтиграфию с технецием-99m (99mTc) [46, 47] и маркированными йодом-123 жирными кислотами [48], которые были полезны при оценке миокардиального саркоидоза.
Сцинтиграфия кости с технецием-99m
Сцинтиграфия имеет высокую чувствительность и несколько меньшую специфичность при оценке процессов, происходящих в кости. Увеличенное поглощение радиоизотопного вещества может быть замечено при разнообразных процессах, таких как метастазы в кости, травмы, инфекции и воспалительные повреждения, включая саркоидоз и дегенеративные повреждения [49]. Частота поражения кости при саркоидозе располагается от 3 до 13 %, хотя, поскольку поражение кости часто бессимптомно, истинная распространенность поражения кости не известна. Мелкие кости рук и ног поражаются более обычно, но может быть поражена любая кость (рис. 3). Наиболее часто саркоидоз кости идентифицируют по присутствию рентгенологических ненормальностей кости у пациентов, у которых саркоидоз уже диагностирован. Однако, дифференциальный диагноз костных повреждения часто бывает трудным [50]. Сцинтиграфия кости с Tc-99m более чувствительна чем рентгенография и сцинтиграфия с 67Ga при обнаружении повреждений костей скелета, вызванных саркоидозом [51]. Yaghmai [52], в ряде из 136 случаев пациентов с саркоидозом с поражением кости продемонстрировал, что сцинтиграфия с Tc-99m позволяет обнаружить на 30 % больше повреждений, чем простая рентгенограмма. По этой причине, истинная частота поражения кости при саркоидозе вероятно недооценена, из-за бессимптомного характера большинства костных повреждений и отсутствия показаний для проведения сцинтиграфии у всех пациентов с саркоидозом. Сцинтиграфия кости с Tc-99m, в отличие от сцинтиграфии с 67Ga, при саркоидозе не способна обнаружить внутригрудные и другие внелегочные локализации [10, 53].
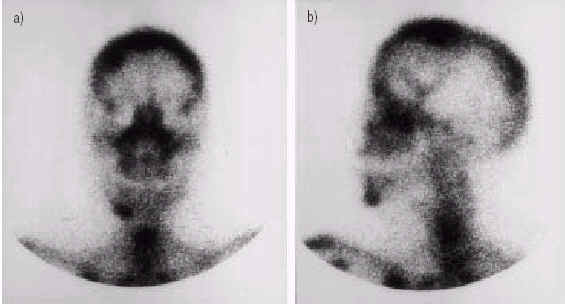
Рис. 3. Радиоизотопная сцинтиграфия кости показывает участки поражения в черепе, нижней челюсти и правой ключице у того же пациента, как на Рис 1: a) фронтальная проекция, b) латеральная проекция. Изображения воспроизведены из [5] с разрешения авторов.
Недавно, Milman с колл. [49] оценили полезность рутинной сцинтиграфии для обнаружения костных и суставных повреждений в группе из 63 белых пациентов с легочным саркоидозом, ни у одного из которых не было симптомов, предполагающих поражение кости. Минорные ненормальности костей, суставов или и того и другого, были обнаружены у 24 (38 %) пациентов. Только один из этих пациентов имел типичные повреждения кости на рентгенограмме. Поскольку диагностическая ценность сцинтиграфии кости при саркоидозе мала, этот метод должен быть сохранен для случаев с симптоматическим поражением костей и для пациентов с патологией рентгенограммы, предполагающей поражение костей или суставов.
Сцинтиграфия с использованием октреотида, меченного радиоактивным индием-111
Сцинтиграфия, использующая 111индий-диэтилентриаминпентаацетиловую кислоту-d-Phe1-октреотид полезна при оценке и лечении нейроэндокринных и злокачественных опухолей [54]. Сообщалось, что нормальные и активизированные лимфоциты и макрофаги экспрессируют рецепторы к соматостатину [55, 56]. Вследствие этого, было предпринято несколько исследований с целью определения полноценности радиоизотопного аналога соматостатина для обнаружения рецепторов соматостатина, экспрессированных на клетках при гранулематозных болезнях, включая саркоидоз.
Ozturk с колл. [57] сообщили об увеличенном поглощении 111In-окреотида в двух случаях саркоидоза. Vanhagen с колл. [55] исследовали полноценность сцинтиграфии рецепторов соматостатина всего тела (SRS) у 13 пациентов с саркоидозом. Локализация гранулем была визуализирована у всех пациентов и дополнительные участки были найдены у 69 %. Кроме того, результаты сцинтиграфии стали отрицательными у 2 пациентов, успешно леченных кортикостероидами, принимая во внимание, что у 3 пациентов, у которых лечение кортикостероидами было неудачным, результаты сцинтиграфии остались положительными. Eklund с колл. [58] оценили полноценность этой методики для обнаружения внелегочных проявлений саркоидоза. Они обнаружили, что 4 из 5 пациентов с саркоидозом имели внелегочную болезнь. Kwekkeboom с колл. [59] проанализировали ценность SRS для оценки активности болезни, предсказания прогноза и корреляции с клиническим курсом у 46 пациентов с саркоидозом. Ранее обнаруженная средостенная, внутригрудная и интерстициальная болезнь была подтверждена у 36 из 37 пациентов. Кроме того, из 7 пациентов с нормальной рентгенограммой, у 5 результаты SRS указывали на коллагеноз. У 13 пациентов, SRS показала ранее необнаруженное внелегочное поглощение радиофармпрепарата, особенно в околоушных железах, надключичных лимфатических узлах, носе, глазах и гранулематозных повреждениях кожи. Поглощение радиоизотопного материала не было замечено у 3 пациентов на участке кожных повреждений, вызванных узловатой эритемой. В целом, SRS позволила обнаружить новые участки болезни у 23 из 46 (50 %) пациентов, но не обнаружила известные участки формирования гранулем, включая кожу, глаза, печень и мозг у 28 % пациентов.
Не было найдено существенной связи между результатом SRS и потребностью в лечении кортикостероидами. Ни степень накопления, ни любой специфический паттерн поглощения, не позволял предсказать прогноз болезни. Результаты SRS обычно коррелировали с прогрессом болезни. У 5 из 6 пациентов, которые имели рентгенографическое улучшение при кортикостероидной терапии, также наблюдалось уменьшение поглощения радиофармпрепарата на скенограмме.
Lebtahi с колл. [60] сравнили SRS с сцинтиграфией с 67Ga при оценке легочной и внелегочной болезни у 18 пациентов с саркоидозом. Сцинтиграфия с 67Ga показала ненормальности у 16 из 18 (89 %) пациентов и обнаружила 64 из 99 (65 %) клинически пораженных участков. Метод SRS обнаружил ненормальности у 18 из 18 (100 %) пациентов и обнаружил 82 из 99 (83 %) клинически пораженных участков. Из 9 леченных пациентов, сцинтиграфия с 67Ga, показала ненормальности у 7 (78 %), обнаружив 23 из 39 (59 %) клинически пораженных участков, принимая во внимание, что метод SRS обнаружил ненормальности у 9 (100 %) пациентов, обнаружив 32 из 39 (82 %) клинически пораженных участков. Однако, 40 % участков внелегочной болезни при использовании SRS было пропущено.
Shorr с колл. [61] изучали 22 пациента с саркоидозом, преобладающе с внутригрудной болезнью и сообщили о сильной корреляции между положительными результатами сцинтиграфии и активностью саркоидоза, особенно рентгенографической стадией и легочной функцией. SRS показала интенсивное поглощение в двух случаях поражения сердца а также в одном случае нейросаркоидоза. Кроме одного пациента с поражением кожни, остальные пациенты не имели клинических свидетельств внелегочного саркоидоза. Однако, они подчеркнули, что SRS не устраняет потребность в проведении биопсии для подтверждения диагноза саркоидоз или исключении злокачественной опухоли. Возможная полноценность октреотидной сцинтиграфии при исследовании кардиосаркоидоза в настоящее время проходит оценку [62].
Сцинтиграфия с 123- мета-йодобензилгуанидином
123- мета-йодобензилгуанидин (MIBG), аналог норадреналина, является радиоизотопным индикатором функционирования симпатических нейронов. Известно, что симпатические нервы сердца связывают 123I-MIBG. Это позволяет визуализировать пресинаптическую симпатическую иннервацию сердца. Сообщалось о ненормальностях при сцинтиграфии с MIBG при саркоидозе [63-65], но, до настоящего времени, основной механизм этого процесса остался неясным. Возможно, местная ишемия или миокардиальное воспаление может играть важную роль. Недавно было обнаружено, что при саркоидозе часто происходит невропатия мелких волокон (SFN) [66].
Миокардиальная дисфункция, оцененная с помощью миокардиальной сцинтиграфии с 123I-MIBG, у пациентов с саркоидозом гетерогенна и зависит от присутствия или отсутствия SFN [71]. В 18 из 47 (38 %) этих случаев, наблюдалось умеренное накопление 123I-MIBG в миокарде.
Позитронно-эмиссионная томография
Роль позитронно-эмиссионной томографии (ПЭТ) всего тела с использованием 18F-флюродеоксиглюкозы (FDG) хорошо известна при лечении пациентов с раком. В последние годы было предположено, что 18F-FDG-ПЭТ также может использоваться при постановке диагноза и лечении пациентов с несколькими типами инфекций, воспалительными процессами и разнообразными доброкачественными болезнями легких [72, 73]. Этот метод основан на обнаружении в экспериментальных исследованиях увеличения метаболизма глюкозы в опухолях и воспаленных тканях [74]. Lewis и Salama [75] первыми описали поглощение 18F-FDG внутригрудными и периферическими лимфатическими узлами при саркоидозе а также кожными повреждениями при узловатой эритеме. Поглощение исчезло после лечения кортикостероидами. Brudin с колл. [76] сообщили об увеличении поглощения 18F-FDG в легких пациентов с активным саркоидозом, что отражает воспалительную активность, которая была подтверждена при биопсии легкого. Sazon с колл. [77] продемонстрировали сильную корреляцию между присутствием поглощения 18F-FDG и активностью саркоидоза, измеренной с помощью обычных процедур.
18F-FDG-ПЭТ также позволила обнаружить рецидив саркоидоза в легком после трансплантации, подтвержденный трансбронхиальной биопсией [78]. Yamada с колл. [79] сообщили, что поглощение 18F-FDG и метионина, меченного 11С при ПЭТ, были полезны для визуализации повреждений у пациентов с саркоидозом. Кроме того, они сообщили, что отношение поглощения 18F-FDG/11С-метионин было полезным для предварительной оценки пациента до лечения. Увеличенное накопление 18F-FDG при саркоидозе впоследствии также наблюдалось другими группами [72, 73]. Однако, одно из главных ограничений 18F-FDG-ПЭТ заключается в неспособности дифференцирования доброкачественных болезней, особенно саркоидоза, от злокачественных. Pitman с колл. [80] предположили, что все массы или узелки с увеличенным поглощением 18F-FDG должны рассматриваться как злокачественные после исключения саркоидоза и туберкулеза.
Alavi с колл. [73] ретроспективно сравнили 18F-FDG-ПЭТ с результатами КТ и описали несколько паттернов поглощения 18F-FDG при саркоидозе, предполагая, они могли бы быть полезны при дифференцировании саркоидоза от злокачественных опухолей. Наиболее обычным паттерном, который наблюдается в 71 % случаев, был так называемый ''типичный'' паттерн, при котором изображение ПЭТ состоит из двустороннего внутригрудного, средостенного и легочного поглощения, подобно замеченному при сцинтиграфии с 67Ga. Эти повреждения коррелировали с результатами КТ и большинство пациентов имели подтвержденный диагноз саркоидоз до проведения ПЭТ.
Второй паттерн был отмечен в 19 % случаев и был назван ''несоответствующим'', потому что ПЭТ показывает множественные очаги интенсивного поглощения, внутригрудные и внелегочные, особенно в селезенке, принимая во внимание, что КТ демонстрирует только отдельные узелки. Этот паттерн был неразличим от изображений, полученных при лимфоме. В присутствии этого паттерна, результаты КТ помогают определить характер повреждений. Злокачественные повреждения обычно растут медленно и часто первоначально видимы только на ПЭТ, но не на КТ. Напротив, воспалительные повреждения являются более метаболически активными, могут быстро изменяться и расти за короткие промежутки времени и вызывать несоответствия, подобно присутствию отдельных или нескольких повреждений на КТ и многочисленных повреждений на 18F-FDG-ПЭТ. Существенное несоответствие между результатами 18F-FDG-ПЭТ и КТ более суггестивно для саркоидоза.
Третий паттерн поглощения 18F-FDG при саркоидозе отмечен в 10 % случаев и называется ''отсутствующая первичная опухоль''. При этом паттерне и КТ и 18F-FDG-ПЭТ показывают множественные мелкие легочные повреждения, суггестивные для метастазов отсутствующей первичной опухоли. Вследствие высокой чувствительности 18F-FDG-ПЭТ при обнаружении злокачественных опухолей, обнаружение множественных ''метастазов'' без обнаружения первичной опухоли, поддерживает диагноз саркоидоз.
Oriuchi с колл. [81] сравнили использование при ПЭТ другого радиоизотопного маркера, 18F-флюро-альфа-метилтирозина (FMT) с 18F-FDG и показали, что хотя и саркоидоз и рак увеличивают поглощение 18F-FDG, только раковые повреждения демонстрировали увеличенное поглощение 18F-FMT. Следовательно, 18F-FMT возможно является более полезным радиоизотопным маркером при ПЭТ, когда саркоидные повреждения должны быть дифференцированы от рака легкого. Поглощение 18F-FDG также происходило на участках внелегочной болезни при саркоидозе, например при поражении кости [82-84], сердца [85] и нервной системы [86].
Степень поражения и определение активности саркоидоза вероятно более точно оценениваются при 18F-FDG-ПЭТ, чем при сцинтиграфии с 67Ga и при других методах визуализации. Кроме того, комбинация 18F-FDG-ПЭТ и КТВР, может помочь лучше дифференцировать активные повреждения от фиброзных. Поэтому, эти методы могут быть полезны при наблюдении некоторых пациентов с саркоидозом. Рис. 4 показывает результаты 18F-FDG-ПЭТ и КТ у пациента с саркоидозом.
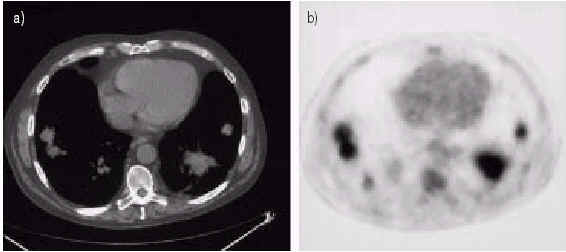
Рис. 4. a) Гибридная КТ и b) 18F-FDG-ПЭТ показали множественные легочные повреждения с высокой интенсивностью метаболизма глюкозы у 63-летнего мужчины с легочным саркоидозом, диагностированным 30 лет назад. Годом ранее у него был диагностирован рак прямой кишки и была проведена операция и лучевая терапия. Биопсия легочных повреждений показала неказеозные гранулемы. Изображения предоставлены C. Gamez и A. Fernandez, PET Unit, Imaging Diagnosis Institute, Bellvitge University Hospital, Barcelona, Spain.
Использование двух изотопов 13N-NH3/18F-FDG при ПЭТ помогло идентифицировать поражение сердца у пациентов с саркоидозом [87]. У 17 пациентов с кардиосаркоидозом была проведена 13N-NH3/18F-FDG ПЭТ. Системный саркоидоз был доказан гистологически. Только 6 пациентов имели миокардиальные дефекты при сцинтиграфии с 201Tl и только 3 имели патологическое накопление 67Ga в сердце. 13 пациентов имели 13N-NH3 дефекты и 14 увеличенное поглощение 18F-FDG в сердце; 12 пациентов имели и 13N-NH3 дефекты и увеличенное поглощение 18F-FDG, два увеличение поглощения 18F-FDG, но не имели 13N-NH3 дефектов и один имел 13N-NH3 дефекты но не имел увеличенного поглощения 18F-FDG. 13N-NH3 дефекты часто наблюдались в базальной антеросептальной стенке левого желудочка, увеличенное поглощение 18F-FDG наблюдалось в базальной и средней части антеросептальной латеральной стенки левого желудочка. Поражение верхушки сердца было редким.
Семь пациентов лечили стероидными гормонами и затем провели дополнительную ПЭТ через 1 месяц после начала стероидной терапии. 13N-NH3 дефекты не демонстрировали никаких существенных изменений после стероидной терапии, принимая во внимание, что поглощение 18F-FDG заметно уменьшилось по величине и интенсивности у 5 пациентов и полностью исчезло у двух. Okumura с колл. [88] сравнили 18F-FDG ПЭТ с результатами сцинтиграфии с 99mTc-MIBI и 67Ga. 10 из 16 пациентов имели различные кардиологические осложнения с тканевым подтверждением при эндомиокардиальной биопсии, например серьезную желудочковую аритмию, атриовентрикулярную блокаду второй и более степени и эхокардиографически доказанную желудочковую дисфункцию. Среди этих пациентов, поглощение 18F-FDG в миокарде наблюдалось у всех пациентов (100 %), значительно чаще, чем при 99mTc-MIBI-SPECT (80 %) и 67Ga сцинтиграфии (50 %).
Хотя патологическое накопление 18F-FDG во многих случаях наблюдалось в областях с уменьшенным поглощением 99mTc-MIBI, участки накопления каждого радиоизотопного маркера часто были независимы. Это несоответствие может отражать воспалительный и дегенеративный процесс в миокарде при кардиосаркоидозе. Недавно, Okumura с колл. [89] продемонстрировали, что 18F-FDG ПЭТ была более чувствительной чем 99mTc- MIBI-SPECT и сцинтиграфия с 67Ga при обнаружении ранней стадии кардиосаркоидоза, который связан с меньшим количеством дефектов перфузии и большей воспалительной активностью до развития существенной сердечной недостаточности.
ПЭТ может иметь большой потенциал при постановке диагноза и лечении кардиосаркоидоза, особенно для пациентов с имплантированным кардиостимулятором или кардиовертором. Однако, большие проспективные исследования, использующие магнитно-резонансную томографию (МРТ), ПЭТ и 111In-окреотид необходимы, чтобы лучше оценить ее роль при оценке кардиосаркоидоза [90].
В будущем, многообещающим могло бы быть использование 68Ga (вместо 67Ga) или 1,4,7,10-tetraazacylcododecane-N,N9,N99,N999-tetraacetic Acid-d-Phe1-Tyr3-octreotide (DOTATOC) [91].
Клинический подход
Лучшими средствами оценки легочного саркоидоза являются рентгенограмма хорошего качества и результаты исследования функции легких (рис. 5). Когда результаты рентгенограммы сомнительны или атипичны для саркоидоза, КТВР используется для изучения средостения и легочной паренхимы. Бронхоскопия с БАЛ и трансбронхиальной биопсией завершает исследование легочного саркоидоза. В этом контексте, ни 67Ga ни другие ядерные методы визуализации не дают более существенной информации.
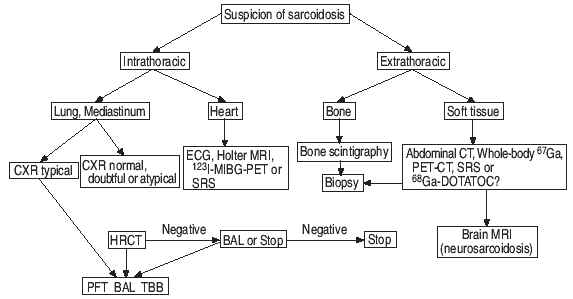
Рис. 5. Алгоритм проведения тестов, который можно использовать при оценке саркоидоза. CXR: рентгенограмма легких; MRI: магнитно-резонансная томография; MIBG: мета-йодобензилгуанидин; PET: позитронно-эмиссионная томография ; SRS: сцинтиграфия рецепторов соматостатина; CT: компьютерная томография; DOTATOC: 1,4,7,10-tetraazacylcododecane -N,N9,N99,N999-tetraacetic Acid-D-Phe1-Tyr3-octreotide; HRCT: КТВР; BAL: бронхоальвеолярный лаваж; PFT: исследование функции легких; TBB: трансбронхиальная биопсия.
Однако, в случаях синдрома Лёфгрена и бессимптомной стадии I с сомнительной внутригрудной лимфаденопатией на рентгенограмме без гистологического подтверждения, обнаружение лямбда-паттерна при сцинтиграфии с 67Ga может вносить вклад в большее доверие к диагнозу. При наблюдении пациентов с легочным саркоидозом, сцинтиграфия с 67Ga может быть полезна при дифференцировании фиброза от активного воспаления, при подтверждении рецидива после прекращения лечения и при оценке активности болезни перед трансплантацией легкого. Комбинация 18F-FDG-ПЭТ и КТ может быть полезной при дифференцировании активной болезни от остаточных фиброзных повреждений в легком. Сцинтиграфия с 67Ga всего тела также весьма полезна в случаях, которые не демонстрируют ненормальностей на рентгенограмме и имеют клиническую картину, суггестивную для изолированного внелегочного саркоидоза, например увеита, болезни центральной нервной системы или моновисцерального гранулематоза неизвестного происхождения, особенно печени или лимфатических узлов. Обнаружение лямбда- и/или панда-паттерна поддерживает диагноз саркоидоз. Сцинтиграфия с 67Ga всего тела также полезна при оценке степени болезни и может указывать на участки для проведения биопсии.
Результаты 18F-FDG-ПЭТ и SRS не специфичны для саркоидоза. Однако, они вероятно лучше оценивают степень поражения и активность саркоидоза, чем сцинтиграфия с 67Ga и другие радиоизотопные методы и могут быть полезны в диагностически трудных случаях. В случае подозрения кардиосаркоидоза, сцинтиграфия с 201Tl может использоваться дополнительно к эхокардиографии, 24-часовому мониторингу и катетеризации сердца с эндомиокардиальной биопсией. Однако, нормальные результаты сцинтиграфии с 201Tl не исключают присутствия поражения сердца. В некоторых центрах в настоящее время вместо 201Tl используется 99mTc-sestamibi. Сообщалось, что 18F-FDG-ПЭТ показала лучшие результаты, чем сцинтиграфия с 201Tl и SRS при исследовании кардиосаркоидоза. Сцинтиграфия с 123I-MIBG может быть полезна при оценке вегетативной дисфункции, которая часто связана с присутствием невропатии мелких волокон (SFN). Недавно было показано, что МРТ является очень точным инструментом при постановке диагноза и лечении кардиосаркоидоза.
Поражение мозга при саркоидозе лучше всего оценивается с помощью МРТ, хотя ядерные методы визуализации также были способны обнаруживать присутствие неврологической болезни. Сцинтиграфия кости весьма чувствительна для обнаружения саркоидных повреждений кости.
Заключение
Ядерные методы визуализации - быстро развивающаяся область, с постоянно появляющимися новыми возможностями. В настоящее время, роль сцинтиграфии при подтверждении диагноза и направления терапии при саркоидозе ограничена. Наиболее часто использующаяся при саркоидозе сцинтиграфия с 67Ga, помогает в определении степени и распределении болезни в диагностически трудных случаях, особенно у пациентов с изолированным внелегочным саркоидозом. Возможно, что степень поражения и определение активности саркоидоза может быть более точно оценена в будущем с помощью 18F-FDG-ПЭТ, особенно в комбинации с КТ или с новыми радиоизотопными маркерами, такими как 68Ga или DOTATOC. Ядерные методы визуализации особенно полезны при наблюдении пациентов для дифференцирования активного воспаления от фиброза.
Резюме
Ядерные методы визуализации играют важную роль в оценке саркоидоза. Некоторые методы доступны в настоящее время, также разрабатываются новые многообещающие методы. Сцинтиграфические методы полезны при дифференцировании фиброза от активной болезни легкого, подтверждении рецидива в сомнительных случаях, при оценке активности болезни перед трансплантацией легкого и при обнаружении поражения сердца других и внелегочных локализаций. Увеличение разрешения изображений при ПЭТ и SPECT, с или без КТ, позволят получить более точное изображение, принимая во внимание, что использование новых радиоизотопных маркеров может дать большее понимание физиологии и степени болезни.
Ключевые слова: сцинтиграфия с 67Ga,сцинтиграфия с 111In-окреотид, сцинтиграфия с 123I-MIBG, позитронно-эмиссионная томография, сцинтиграфия кости с Tc-99m, сцинтиграфии с 201Tl.