Current Opinion in Pulmonary Medicine 2002
Эпидемиология саркоидоза: новые границы исследования
Yutaka Hosoda, MD, Radiation Effects Research Foundation, Hiroshima, Hiroshima; Sumiko Sasagawa, PhD, Institute for Environmental Sciences, Rokkasho, Aomori; Norikazu Yasuda, PhD; National Institue of Radiological Sciences, Inage, Chiba, Japan.
Начиная с 1990 г., в базы данных Medline и PubMed было добавлено более 100 сообшений по эпидемиологии саркоидоза. Из них лишь несколько были опубликованы позднее марта 2001 г. Эта статья сосредоточена на работах, опубликованных после этой даты, а также на предыдущих важных эпидемиологических исследованиях. Обзор построен согласно двум главным эпидемиологическим категориям: (1) факторы, связанные с хозяином - возраст, пол, раса, семейная группировка и образ жизни; и (2) факторы, связанные с временем и местом - внешнее воздействие, географические факторы, местная группировка, климатические и сезонные вариации, миграция и время-пространственная группировка (трансмиссия).
Введение
Различные эпидемиологические факторы, связанные с саркоидозом, описанные между 1950 г. и 2001 г. внесены в Таблицу 1. Однако, отдельно взятые факторы не являются независимыми элементами и сложно взаимодействуют между собой и инициирующим фактором.
Таблица 1
| Факторы, связанные с хозяином | Факторы, связанные с временем и местом |
| Возраст и пол | Внешнее воздействие |
| Раса | Географические факторы |
| Семейная группировка | Местная группировка |
| Образ жизни | Климатическая и сезонная группировка |
| Миграция | |
| Время-пространственная группировка |
Факторы, связанные хозяином
Возраст и пол
ATS/ERS/WASOG Statement [1] описывает саркоидоз как ''болезнь, со склонностью у взрослых в возрасте до 40 лет, с пиком в возрасте 20-29 лет. В Скандинавских странах и Японии имеется второй пик заболеваемости у женщин возрасте более 50 лет. Большинство исследований указывает на немного более высокую заболеваемость болезни у женщин.'' Однако, тщательный обзор предыдущих эпидемиологических исследований показал наличие второго пика заболеваемости у женщин в возрасте более 50 лет и в других странах, как показано в исследовании в 1966-1975 в Rochester [2] и в Английском исследовании 1961-1966 [3]. В Японии, в 1960-х годах, возраст-специфическая заболеваемости имела вид монотонной кривой с пиком в 20 лет у обоих полов. В период 1960-1990, однако, было показано, что заболеваемость имеет вид двухвершинной кривой с пиками в возрасте 20 и 50 лет. Хотя у мужчин пик был больше в 20 лет, чем в 50, у женщин пик оказался выше в 50, чем в 20 лет [4-6]. Эти результаты показывают, что восприимчивость хозяина к саркоидозу достигает максимума в эти два периода жизни.
Раса
О значительно большем риске саркоидоза у чернокожих по сравнению с белыми было сообщено во многих американских исследованиях. В US Navy (военно-морские силы США), OR (чернокожие по сравнению с белыми) был 7.5 (95 % CI, 6.3-8.9) в период 1981-1995 [7]. В Мичигане [8], ежегодная заболеваемость на 100,000 была 35.5 у чернокожих и 10.9 у белых. В расово смешанном сообществе Лондона, ежегодная заболеваемость на 100,000 была 4 для британцев, 21 для ирландцев, 58 для индусов и 14 для азиатов [9]. Считается, что такие расовые различия определяются генетическими факторами [8].
Семейная группировка
О семейной группировке саркоидоза также неоднократно сообщалось, начиная с 1920 г. Распространенность семейного саркоидоза располагается от 1.7 % в Великобритании [10] до 9.6 % в Ирландии [11] и может достигать 14 % [12-14]. Интересным является сравнение семейного саркоидоза в Финляндии и на острове Хоккайдо, в Японии. Хотя распространенность саркоидоза в Финляндии приблизительно в восемь раз выше чем на Хоккайдо, распространенность семейного саркоидоза между этими двумя странами различалась не настолько сильно : 3.6 % в Финляндии и 4.3 % на Хоккайдо [15]. В расширенном исследовании [6], частота семейного саркоидоза была выше в Furano (область Хоккайдо) чем в целом на Хоккайдо (4 семьи из 46 случаев - 8.7 % по сравнению с 21 семьей из 700 случаев - 3 %, p = 0.049). Эта местная группировка, возможно, связана с кровными браками в небольшом регионе, вместе с хорошей регистрации случаев саркоидоза. В исследовании ACCESS, относительный риск саркоидоза был оценен, используя анализ 10,862 родственников первой степени родства, 17,047 родственников второй степени и 706 индивидуумов в группе контроля, согласованных по возрасту, полу и географическим факторам [16]. Согласно результатам логистического регрессионного анализа, родные братья/сестры имели самый высокий относительный риск (OR, 5.8; 95 % CI, 2.1-15.9), с меньшим ристком у дядей/тетей, бабушек/дедушек и родителей (3.8; 1.2-11.3). Белые имели заметно более высокий семейный относительный риск по сравнению с чернокожими (18.0 по сравению с 2.8, P = 0.098).
Риск семейного саркоидоза был оценен в 179 чернокожих семьях в США [16]. 12 из 327 (3.7 %) родных братьев/сестер и 11 из 161 (6.8 %) родителей сообщили об истории семейного саркоидоза.
Риск семейного саркоидоза среди близких родственников в этом исследовании был 2.24 (95 % CI, 1.16-3.92) для родных братьев/сестер и 2.82 (1.41-5.12) для родителей. При объединении родных братьев/сестер и родителей, семейный риск был 2.49 (1.58-3.73). Было сделано заключение, что чернокожие родные братья/сестры и родители c саркоидозом имеют в 2.5 увеличенный раза риск саркоидоза и что среди членов семьи может существовать гетерогенность риска болезни. Другое исследование риска семейного саркоидоза в Великобритании [17] показало, что 24 (5.9 %) из 406 пациентов имели по крайней мере одного родственника (второй или третьей степени родства) с доказанным биопсией саркоидозом. Риск для родных братьев/сестер пациентов с саркоидозом был определен между 36 и 73 (по сравнению со всей популяцией), указывая на значительную семейную группировку болезни. Авторы поддерживают теорию, в которой общий фактор (генетический или из окружающей среды) является причиной семейного саркоидоза и предполагают, что этот фактор является общим для всех этнических групп.
Образ жизни
Связь саркоидоза с образом жизни также была изучена в нескольких исследованиях, но каких-либо значительных связей между образом жизни и саркоидозом обнаружено не было [18-20]. Исключением, как сообщается в исследовании [21], является курение. Иследование показало значительно более низкий процент курящих (21.9 %) среди 202 пациентов с саркоидозом чем в обзоре семей во всей популяции. Исследование географических вариаций саркоидоза и социально-экономического статуса в Южной Каролине [22] показало, что по крайней мере в этом регионе, область, расположенная вдоль береговой линии Атлантического океана, связана по крайней мере с одной количественной характеристикой саркоидоза и что для чернокожих существует географический фактор риска развития саркоидоза.
Факторы, связанные с временем и местом
Внешнее воздействие
ВМФ США. Флот США провел обширные эпидемиологические исследования, чтобы выяснить, связаны ли с саркоидозом любые внешние воздействия на судах ВМФ США [7,23,24]. Первый отчет [23] о 426 случаях, показал высокий риск саркоидоза у служащих авианосцев RR = 1.47 (95 % CI, 1.2-1.9); и у чернокожих по сравнению с белыми RR = 8.2 (6.7-10.0) в период 1971-1993 г. Второй отчет [24], используя анализ 1220 случаев саркоидоза и 10,000 индивидуумов в группе контроля в период 1943-1993 г., показал, что для чернокожих OR был 8.6 (7.5-10.0). Кроме того, фактором, защищающим от развития саркоидоза, была служба на ''чистом судне'' (не индустриальные суда) OR = 0.06 (0.00-0.27) для чернокожих и 0.37 (0.13-0.84) для белых. В третьем отчете [7], был обнаружен увеличенный риск госпитализации с саркоидозом для морских пехотинцев OR = 1.4 (1.2-1.8), для чернокожих по сравнению с белыми 7.5 (6.3-8.9), для военнослужащих в возрастк 32 года по сравнению с возрастом 17-21 год 5.0 (3.5-7.3), в период 1981-1985 г. по сравнению с 1991-1995 г. 1.7 (1.4-2.1) а также для проживания до призыва на службу в юго-восточных регионах США по сравнению с юго-западными 2.2 (1.6-2.8). Авторы первого отчета упоминают, что связь развития саркоидоза с назначением на авианосцы предполагает профессиональный фактор, так как назначение на этот тип судна - плохая замена любого специфического воздействя, которое могло бы быть связано с болезнью. Как будет показано ниже, миграция - важный фактор в эпидемиологии, и служба на флоте может быть расценена как иммиграция в замкнутую окружающую среду суда. Дальнейшие исследования этой группы пациентов может внести ценный вклад в изучение этиологии саркоидоза.
Пожарные. Два отчета сообщили об увеличенном риске саркоидоза среди пожарных [25,26]. Одиннадцать тысяч пожарных Нью-Йорка наблюдалась в течение 14 лет (1985-1998) вместе с группой контроля, состоящей из 3000 работников скорой помощи, наблюдаемой в течение 4 лет (1995-1998) [26]. Среди пожарных было 94 % белых, по сравнению с 44 % среди работников скорой помощи. Ежегодная заболеваемость для пожарных составила 2.9 на 100,000 при общем количестве 25 случаев и 0 в группе контроля. Однако, было отмечено, что работники скорой помощи не являются согласованной группой контроля в отношении размера группы (меньше), периода наблюдения (короче) и по отсутствию случаев болезни в группе контроля.
Сельское хозяйство. В США было предложено множество воздействий - песчаной почвы [27], глины [28], сосновой пыльцы [29] и т.д., как причины саркоидоза. Недавнее исследование [30], показало связь саркоидоза с воздействием продуктов горения от каминов и печей, которые топят дровами, что поддерживает гипотезу, что образ жизни, связанный с проживанием в сельской местности может играть определенную роль в развитии саркоидоза. Необходимы дальнейшие исследования с большим количеством случаев болезни, чтобы подтвердить эту гипотезу.
Медицинский персонал. Имеется несколько отчетов [31-33] о более высокой заболеваемости саркоидозом среди работников здравоохранения. При интерпретации этих данных необходимо учитывать, что работники здравоохранения могут иметь большую доступность медицинского обслуживания.
Географические вариации
Глобальные географические вариации имеют общую тенденцию - ''чем дальше от экватора, тем больше количество пациентов с саркоидозом [34]''. В Европе, Скандинавские страны имеют намного более высокую заболеваемость чем другие Европейские страны. В США, многие исследователи [7,23,35,36] признали географическую группировку пациентов в южных или центральных штатах, как по месту жительства, так и по месту рождения. Интересно, что американские исследования не показали никаких географических вариаций в зависимости от места рождения при оценке заболеваемости приблизительно 30 лет назад, когда пациенты были рождены [37]. Среди штатов США, эта болезнь настолько редка на Гавайях, что сообщалось только об одном случае саркоидоза [38]. Среди всех индустриально развитых государств, Канада - единственная страна, для которой эпидемиологических данных нет.
Местная группировка
Имеется несколько сообщений о местной группировке болезни [5,6,31]. В некоторых областях Швеции, частота легочного саркоидоза превышает 100 на 100,000 [5]. В Японии, 22-летняя регистрация (1973-1994) случаев саркоидоза в Furano (маленький город с населением 10,000 человек, расположенный в центре острова Хоккайдо), показала увеличенную в 10-20 раз заболеваемость саркоидозом: от 10.2 на 100,000 (1973-1983) до 23.3 (1984-1994) [6], хотя заболеваемости во всей Японии составляет 1.0 на 100,000 [5].
Климат и сезонные вариации
О сезонных вариациях начала саркоидоза сообщалось в обоих полушариях. Пиковые месяцы начала - март/май в Лондоне, [39] март/апрель в Афинах [40], январь/июнь в Финляндии, апрель/июнь в Барселоне [41], апрель/август в Японии [4] и весенние месяцы (август - декабрь) в Новой Зеландии [42]. С точки зрения климата (Атлас мира, Оксфорд, 1973), самая высокая распространенность саркоидоза наблюдается в странах с холодным летом и умеренной зимой (Европа) или с умеренным летом и зимой (юго-восточные штаты США). Хотя Канада расположена в климатической зоне с холодным летом и холодной зимной, данных о заболеваемости для этой страны в настоящее время нет [4].
Миграция
Миграция - важный фактор в эпидемиологии, связаный с влиянием новой окружающей среды и образа жизни. Исследование иммигрантов в Лондоне в период 1958-1976 г., показало более высокую распространенность саркоидоза среди иммигрантов: 27 на 100,000 среди женщин, рожденных в Лондоне, 213, среди женщин, рожденных в Ирландии и 170 среди британско-карибских женщин. Это исследование предполагало влияние как миграции, так и различной этнической восприимчивости [43]. В Японии [34], самая высокая распространенность саркоидоза наблюдается на Хоккайдо, большом северном острове, на который большинство жителей мигрировали из Японии в 1870 г. Приблизительно 80 % жителей Хоккайдо происходят из северной части Японии. Коренные жители острова - айны (Ainu), почти все вымерли, главным образом от инфекционных болезней. Высокая распространенность саркоидоза на Хоккайдо, поэтому, наблюдается при сравнения заболеваемости у потомков эмигрантов на Хоккайдо и оставшихся жить в Японии. Имеется аналогия с потомками чернокожих эмигрантов с Африканского континента и оставшихся жить в Африке. В этом отношении, доступным является только отчет из Кейптауна [44], который показал, что распростаненность саркоидоза составляет на 100,000 - 27 у чернокожих, 6 у белых и 17 у метисов, но сравнительных исследований между чернокожими на этих двух континентах не проводилось.
Время-пространственная группировка (трансмиссия)
Несколько исследований указали на существование время-пространственной группировки [25,45]. Исследование на острове Мэн показало наличие значительной связи между случаями саркоидоза, разделенными интервалом времени менее 10 лет и расстоянием менее 100 метров друг от друга. Это исследование, однако, критикуется по трем пунктами [8]: (1) отсутствие супружеских пар среди 49 контактов пациент-пациент, (2) девять пар были кровными родственниками, и (3) число коренных жителей острова Мэн было выше, чем ожидалось. Эксперты считают, что эти данные являются совместимыми с наследственным риском саркоидоза. В узком смысле, время-пространственная группировка наблюдается при трансплантации органов [46,47]. Пациенты с саркоидозом, у которых проводилась трансплантация сердца и легкого от доноров без саркоидоза, имели рецидив саркоидоза в аллотрансплантах легкого после операции. У пациента без саркоидоза, которому была проведена трансплантация сердца от донора с саркоидозом, при трансбронхиальной биопсии были обнаружены гранулемы и интерстициальное воспаление в легком [48].
Что было сделано в прошлом, что происходит в настоящее время и что должно быть сделано в будущем
Что было сделано
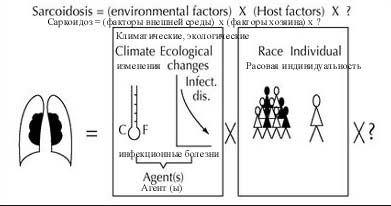
В течение второй половины 20-го столетия, были накоплены эпидемиологические данные, чтобы раскрыть эпидемиологические особенности саркоидоза, которые позволили выделить факторы окружающей среды и факторы хозяина. Гипотетическая схема саркоидоза (рис. 1), созданная в прошлом веке, все еще является основной концепцией, которая будет исследоваться сложными современными научными методами.

Рис 1. Гипотетическая схема саркоидоза. Старая, но все еще применяемая схема изучения причин саркоидоза с помощью сложных современных методов.
Что происходит в настоящее время
Поскольку саркоидоз - системная болезнь, требуются мультидисциплинарные исследования. WASOG, организованная Om P. Sharma и G. Rizzato и журнал, ''Sarcoidosis, Vasculitis, and Diffuse Lung Diseases'' под редакцией D.J. James и G. Semenzato, играют ведущую роль в исследовании саркоидоза. Среди индивидуальных исследований выделяется крупное американское мультицентровое исследование саркоидоза ACCESS, начатое в 1996 г., чьи результаты будут опубликованы в ближайшем будущем [16, 49-51].
Что должно быть сделано в будущем
Эпидемиология не является исследованием, позволяющим идентифицировать агент, вызывающий саркоидоз, но может направить ученых в правильном направлении, при поддержке новых медицинских технологий. Однако, любые положительные и отрицательные результаты должны тщательно интерпретироваться. Статистически значимый результат не всегда означает причинную связь, также как отсутствие доказательств связи - не доказательство ее отсутствия [52]. В 21 столетии ожидается получение новых результатов: через всестороннее изучение эпидемиологии генома человека, обнаружение провоцирующего агента и факторов восприимчивости хозяина к саркоидозу.