Respir Med 2000 Aug;94(8):815-820
Связь воздействия искусственных минеральных волокон и саркоид-подобных гранулем
Drent M, Bomans PH, Van Suylen RJ, Lamers RJ, Bast A, Wouters EF
Departments of Pulmonology, Electronic Microscopy, Pathology, Radiology, Pharmacology and Toxicology, University Hospital Maastricht, The Netherlands
Реферат
Считается, что саркоидоз вызван воздействием ингаляционных агентов, переносимых воздухом и вызывающих воспалительную реакцию у восприимчивых людей. Связь воздействия бериллия, алюминия и других металлов с развитием саркоид-подобной легочной болезни хорошо известна. Способность искусственных минеральных волокон (MMMF) производить гранулематозную болезнь легкого до сих пор не была оценена. Недавно мы наблюдали связь саркоид-подобной гранулематозной реакции и истории профессионального воздействия стекловолокна. Мы выдвинули гипотезу, что имеется связь между воздействием MMMF и развитием саркоид-подобных гранулем. Мы рассмотрели истории болезни 50 пациентов с саркоидозом, наблюдавшихся в нашей клинике в период 1996-1999 г. В 14 случаях пациенты сообщили об истории воздействия стекловолокна или асбеста. Были рассмотрены доступные гистологические препараты (n = 12). В 6 случаях качественный анализ с помощью электронной микроскопии показал фрагменты кварца, алюминия и иногда титана. Была обнаружена связь между накоплением волокон и гранулемами. Эти результаты указывают, что у восприимчивых индивидуумов воздействие MMMF может быть связано с хронической гранулематозной болезнью, подобной хронической бериллиевой болезни.
Введение
Хотя причина саркоидоза остается неизвестной, имеются свидетельства, поддерживающие идею, что саркоидоз происходит при воздействии на наследственно восприимчивых хозяев специфических агентов окружающей среды, вызывающих воспалительную реакцию (1). Некоторые инфекционные агенты, например вирусы, Proprionibacterium acnes и микобактерии рассматривались как потенциальные причины саркоидоза. Неинфекционные неорганические и органические агенты окружающей среды могут вызывать гранулематозный ответ с особенностями, которые являются подобными саркоидозу (1).
Связь воздействия металлов, таких как бериллий и саркоид-подобной легочной болезни, хорошо известна (1,2). Подобными свойствами также обладают другие металлы, такие как алюминий, цирконий, титан, редкоземельные металлы (церий) а также тальк, который содержит алюминий и кварц (1,3-7). Поскольку многие агенты различной природы, инфекционные, органические и неорганические, могут вызывать гранулематозный ответ у восприимчивых индивидуумов (1-7), весьма вероятно, что единственной причины саркоидоза не существует. Поэтому, является важным поиск любого возможного билогически уместного воздействия на пациента с подозреваемым саркоидозом. Недавно мы наблюдали присутствие саркоид-подобных гранулем у пациента с историей воздействия стекловолокна (8). Эта связь побудила нас оценить, связано ли воздействие различных MMMF, таких как асбест или стекловолокно, с развитием саркоид-подобного гранулематозного ответа.
Пациенты
Мы рассмотрели истории болезни 50 пациентов с саркоидозом, наблюдавшихся в нашей клинике в период 1996-1999 г. Всех пациентов опрашивали относительно их медицинской истории, с особым вниманием к любому воздействию профессиональных факторов и/или факторов окружающей среды. Опрос показал, что 14 пациентов имели историю воздействия асбеста или стекловолокна (группа I). Чтобы определить возможную связь воздействия MMMF и развития саркоид-подобных гранулем, были исследованы гистологические препараты этих пациентов с саркоидозом, которые были доступны для 12 из 14 пациентов.
Результаты
При опросе, 6 пациентов сообщили, что они работают или работали в прошлом до развития саркоидоза на одной и той же фабрике по производству асбеста. Еще 2 пациента контактировали с асбестом в течение многих лет. Кроме того, шесть пациентов имели контакт со стекловолокном. Ни один из этих пациентов никогда не использовал респираторы или любые другие средства индивидуальной защиты, чтобы уменьшить количество вдыхаемых MMMF. Таким образом, 14 пациентов имели историю воздействия MMMF (группа I). Остальные 36 пациентов (группа II) не помнило о воздействии MMMF.
Средний серологический уровень АПФ, уровни С-реактивного белка, кальция, мочевой кислоты были увеличены у всех пациентов. Кроме того, неспецифическое увеличение уровней иммуноглобулинов было отмечено у 7 пациентов в группе I. Анализ ЖБАЛ показал паттерн, характерный для саркоидоза с увеличенным полным индексом клеток, с преобладанием лимфоцитов (12). Отношение CD4/CD8 было 3.4±3.8 в группе I и 4.7±3.6 в группе II, соответственно. Никаких статистических различий при анализе ЖБАЛ между группами найдено не было.
Согласно критериям American Medical Association, в группе I наблюдалось умеренное ухудшение функции легких (60-80 % от должного). Три пациента имели более серьезное ухудшение (40-60 % от должного). Десатурация при физической нагрузке была обнаружена у 8 пациетов (57.1 %) группы I и у 10 пациентов (27 7 %) группы II. Все пациенты имели усталость, сухой кашель, одышку при физической нагрузке, боль в груди, иногда артралгии, потерю веса, ночную потливость и лихорадку.
На основании серьезности болезни, которая оценивалась по результатам исследования функции легких, присутствию десатурации при физичесой нагрузке, рентгенографической стадии и особенностей КТ, у всех пациентов группы I и у 11 пациентов (30.5 %) группы II проводилось лечение преднизоном. Однако, после снижения дозировки перднизона произошел рецидив у 13 пациентов в группе I (92.8 %) и у 7 пациентов в группе II (19.4 %). У 4 пациентов группы I и у 1 пациента группы II симптоматического улучшения не произошло, несмотря на лечение кортикостероидами. Радиологические ненормальности и функция легких ухудшились. Поэтому, у 3 пациентов группы I и у 1 пациента группы II было начато лечение циклофосфамидом (100 милиграмм ежедневно), У одного пациента группы II проводилось лечение метотрексатом (15 милиграмм один раз в неделю). Наблюдение за респираторными симптомами и клиническими проявлениями показало, что нелеченные пациенты группы II (n=25) имели спонтанную ремиссию (n=18) или не имели ухудшения (n=7), в отличие от ни одного пациента из группы I.
Были исследованы доступные гистологические препараты 12 пациентов группы I (ткань легкого, n=11; ткань средостенного лимфатического узла, n=1). Во всех образцах ткани легкого, основным компонентом были подслизистые, интерстициальные и иногда субплевральные, не сливные ненекротические гранулемы. В некоторых гранулемах наблюдались многоядерные гигантские клетки Лангерганса или гигантские клетки инородных тел.
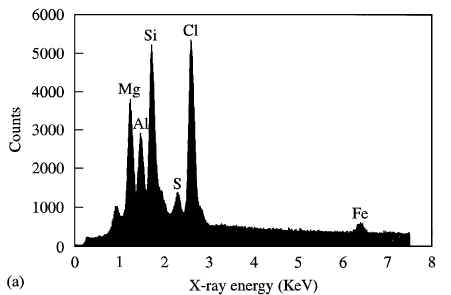
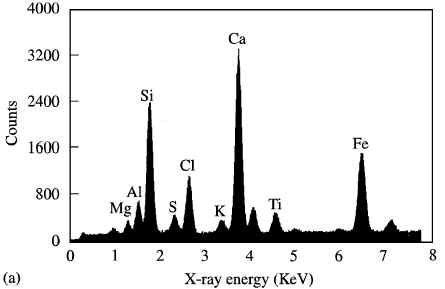
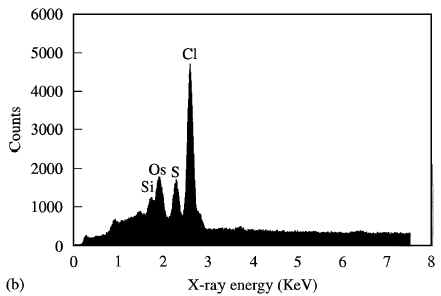
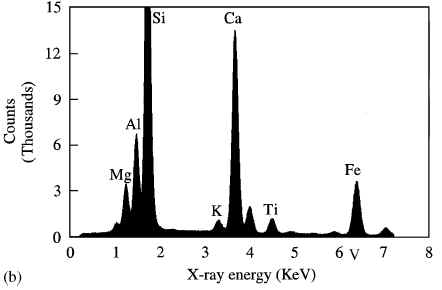
Качественный анализ с помощью электронной микроскопии фрагментов гранулем по типу ''инородное тело'', показал наличие кварца, алюминия и иногда титана (рис. 1a и рис. 2a). Этот спектр отличался от ткани легкого без гранулем по типу ''инородное тело'' (рис. 1b). На рис. 2b показан спектр асбеста.
|
|
| Рис. 1а. Спектр волокон из ткани легкого пациента, который подвергался воздействию стекловолокна. На спектре видны пики соответствующие магнию (1.253 keV), аллюминию (1.486 keV) и кремнию (1,740 keV). Пики, соответствующие сере и хлору происходят из вспомогательного материала, используемого для консервации образцов ткани. | Рис. 2а. Спектр волокон из ткани легкого пациента, который подвергался воздействию асбеста. На спектре видны пики соответствующие магнию (1.253 keV), аллюминию (1.486 keV) и кремнию (1,740 keV), калию (3.313 keV), кальцию (3.691 keV), титану (4.509 keV) и железу (6.899) KeV. Пики, соответствующие сере и хлору происходят из вспомогательного материала, используемого для консервации образцов ткани. |
|
|
| Рис. 1b. Спектр смежной области легочной ткани, не содержащий гранулем. | Рис. 2b. Спектр асбеста. |
Обсуждение
Обзор профессиональной истории 50 пациентов с саркоидозом показал воздействие MMMF у 14 пациентов. Дисперсионный анализ 7 экземпляров биопсии показал наличие кварца, алюминия и титана, которые входят в состав асбеста (рис. 2b). Поэтому, мы считаем, что мы идентифицировали потенциальный профессиональный фактор окружающей среды, который связан с увеличенным риском развития саркоидоза у генетически восприимчивых людей. Разработка специфического теста пролиферации лимфоцита в ответ на MMMF, подобному ранее разработанному для бериллия, позволило бы подтвердить эту гипотезу.
Однако, такой тест разработать очень трудно, поскольку MMMF содержат различные элементы, включая алюминий, кварц и титан. Возможно, кожные пробы позволят обнаружить специфические реактивные IgE антитела. Кроме того, генетическое типирование может позволить идентифицировать возможные факторы генетической восприимчивости. Кроме того, необходимо собрать информацию о количестве рабочих, подвергнутых воздействию MMMF и о количестве рабочих, у которых в конечном счете разовьется саркоид-подобная болезнь. Будущие исследования должны проводиться в группе подвергнутых воздействию MMMF рабочих и в контрольной группе, чтобы идентифицировать частоту саркоидоза в обоих группах.
Исследование рабочих, занятых на производстве MMMF, проведенное Hughes с коллегами (13) не показало влияния MMMF на дыхательную систему (13). Хотя сообщалось о связи воздействия MMMF и развития легочного фиброза (14-16), связь MMMF и развития гранулематозной болезни легкого на настоящего времени не оценивалась (16). Известно, что гранулемы исчезают, когда болезнь прогрессирует к фиброзу. Рассматривалась связь воздействия инородных тел и развития легочного саркоид-подобного гранулематоза с T-клеточным альвеолитом (17). Морфологически, эти гранулемы неразличимы от ненекротических гранулем, встречающихся при саркоидозе. Day с коллегами предложили, что воспалительный ответ, индуцированный присутствием минералов в легочной ткани, может вызывать изменение иммунорегуляции, что приводит к патологическим изменениям в ткани (18). Металлическая пыль может действовать как антиген в аллергической реакции (2-7).
Jacket с коллегами установили покровные стекла в легких крыс линии Wistar и наблюдали неспецифическое накопление макрофагов в альвеолах и иногда гранулематозную реакцию (19). Оценка цитотоксичности, воспалительного и/или фиброгенетического ответа позволила предположить, что повреждение ДНК могло быть связано с производством гидроксильных радикалов, которое происходит при взаимодействии металлических частиц с плазматической мембраной клеток (2). Поверхность MMMF также может стимулировать производство гидроксильных радикалов и поэтому может быть фактором, стимулирующим окислительный стресс, вызывающим нарушение баланса между генерацией свободных радикалов и скавенджерными реакциями (20). Gilmour с коллегами показали способность MMMF производить свободнорадикальные реакции на поверхности волокна (21). Кроме того, Driscoll с коллегами описали активацию NFkappaB частицами кварца (22). Недавно мы продемонстрировали активацию NFkappaB при саркоидозе (23). Сообщалось, что кремнезем индуцировал производство фактора некроза опухоли альвеолярными макрофагами к крыс. Обнаружение свободнорадикальной активности на поверхности волокон с неизвестной токсичностью, поддерживает утверждение, что волокно является токсичным; однако, отсутствие свободнорадикальной активности не может быть принято как свидетельство нетоксичности (24,25).
При производстве изоляционных материалов используется более 80 % от общего производства MMMF. Они используются при производстве огнеустойчивой тепловой и акустической изоляции, в подвесных потолках и стеновых панелях, в системах кондиционирования и вентиляции а также в садоводстве (14). При производстве MMMF используется стекло, шлак, каолиновая глина или смесь кремнезема и окиси алюминия.
При оценке потенциальных рисков для здоровья должны рассматриваться концентрация волокон в воздухе, химический состав и размер волокон. Чтобы достигать альвеол, волокна должны иметь определенный размер (<10 мкм, связано с аэродинамикой) (14). В некоторых исследованиях, патогенные свойства MMMF были связаны с их накоплением и персистированием в целевых органах (13,15). Фактически, это главная опасность при оценке токсичности MMMF, так как весьма вероятно, что эти волокна не могут быть быстро выведены из легких. Raffinsson с коллегами указали на связь между саркоидозом и воздействием кристобалита (26). Barbazza с коллегами предположили, что развитие гранулем после ингаляции частиц кварца не зависело от количества кварца, но было связано с индивидуальным клеточным ответом (27). Имеются свидетельства, например полученные при исследовании бериллиоза, что гранулематозный ответ на органические и неорганические стимулы требует некоторой формы предрасположенности хозяина. Кроме того, хроническая бериллиевая болезнь происходила и при высоких и при низких уровнях воздействия бериллия, без явной корреляции между величиной воздействия и заболеваемостью (2). Поэтому, возможно, не только количество, но и качественый состав (компоненты волокон) связан с развитием гранулематозных реакций у наследственно восприимчивых индивидуумов. Richeldi с коллегами обнаружили, что у индивидуумов, подвергнутых воздействию бериллия, маркер HLA-DPB1 Glu был связан с увеличением в 8 раз частоты развития болезни в группе рабочих с историей более высоких уровней воздействия бериллия. Поэтому, генетические факторы могут иметь добавочный или мультипликативный эффект. Такая модель бериллиоза указывает, что генетические исследования могут быть полезны для определения рисков для различных уровней воздействия на наследственно восприимчивых индивидуумов (28). Эти наблюдения могут иметь серьезное значение, поскольку защита от воздействия MMMF недостаточна и многие люди подвергаются воздействию MMMF даже не зная об этом.